
图说:化学与分子工程学院、上海市绿色化学与化工过程绿色化重点实验室步文博教授。图片来自华师大新闻中心
所谓“肿瘤饥饿疗法”就是切断肿瘤血管、饿死癌细胞,但这一理论自问世以来一直受困于其对无机材料的苛刻要求。华东师范大学15日宣布,该校科研人员开创性地提出了无机耗氧剂用于肿瘤饥饿疗法的新思路,为传统的肿瘤饥饿疗法注入了新活力。
这项在线发表在国际著名学术期刊《自然-纳米技术》上的成果,是由华东师大化学与分子工程学院、上海市绿色化学与化工过程绿色化重点实验室步文博教授团队与中科院上海硅酸盐研究所研究员施剑林课题组合作完成的。
1971年,美国哈佛大学教授佛克曼首次提出切断肿瘤血管、饿死癌细胞理论,即没有血管的肿瘤在一个月的时间里连1毫米都长不到,拥有血管的肿瘤3天就能长到原来体积的16000倍。“肿瘤”与“血管”的关系是“树”与“根”、“鱼”与“水”的关系,“血管”就是肿瘤的“命门”,破坏或者清除肿瘤的血管,肿瘤必然死亡。饿死癌细胞的这一抗癌全新思路、全新疗法石破天惊,让世界都为人类最终战胜癌症而奔走相告。从此世界各国科学家投入大量人力财力,进行该方面研究和开发。美方有研究表明,在癌症患者中约有10%的人会发生肿瘤自然消失,并极少复发的现象,癌症自然消退的根本原因,就在于肿瘤血管被破坏。然而遗憾的是,由于“肿瘤饥饿疗法”对无机材料的苛刻要求,需要满足肿瘤组织的特异性、耗氧能力强、阻塞血管持久性,可注射性、良好的生物相容性等要求,目前的无机材料用于肿瘤饥饿疗法还无法实现。
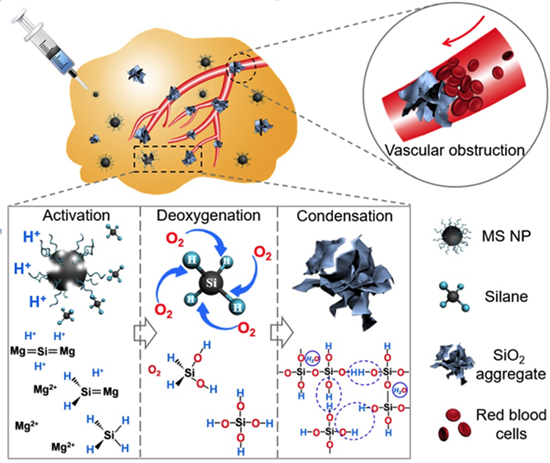
图说:肿瘤饥饿疗法示意图。图片来自华师大新闻中心
步文博教授及其团队同事的研究,是从采用自蔓延燃烧方法合成新型Mg2Si纳米颗粒出发,从而揭示了肿瘤微环境可以特异性激活Mg2Si纳米颗粒的耗氧功能和分解产物堵塞肿瘤血管的新现象。他们采用改进的自蔓延燃烧法,成功制备了单分散、直径约100nm的硅化镁(Mg2Si)纳米耗氧剂,经聚乙烯吡咯烷酮(PVP)表面改性后形成稳定的溶胶,赋予其良好的可注射性。
实验结果显示,该新型耗氧剂在肿瘤组织弱酸性微环境下被特异性激活,利用中间产物硅烷(SiH4)快速高效、持久消耗肿瘤组织及血管中的溶解氧和血红蛋白结合氧,导致肿瘤病灶区极度缺氧;更重要的是,耗氧剂的分解产物SiO2在肿瘤组织血管中原位自聚集形成微米级絮状物,高效率阻塞肿瘤血管,切断肿瘤周围的氧分子和营养成分通过肿瘤血管系统的供给,同时也切断了肿瘤侵袭、转移的血管途径,致使癌细胞发生明显的纤维化、凋亡和坏死,达到“饿死肿瘤”的治疗效果;值得一提的是,该策略采用的制备工艺可以批量化、低成本制备硅化镁耗氧剂,并仅能在肿瘤病灶区特异性激活其耗氧功能,正常组织和器官中无法激活其耗氧功能,该类不含有重金属离子的新型耗氧剂,不但自身具有良好的生物相容性,其分解产物(Mg2+和SiO2)同样也无毒无害,并最终被安全地代谢出体外,克服了医用无机材料难降解、活体内滞留易导致生物毒性的医学难题。该工作为批量化制备新型功能纳米材料提供了新的方法,同时为“肿瘤饥饿疗法”提供了新的思路。(新民晚报首席记者王蔚)